Atomer og det periodiske system
Protonerne og neutronerne sidder inde i kernen, mens
elektronerne sidder ude på skallerne. Elektrontallet kan variere, men det kan
protontallet ikke - det gør at man kan se atom nr./grundstofs nr. på hvor mange
protoner der er i inde i atomet.
6 HE - Nukleantal er antallet af atomer inde i kernen (protoner og neutroner)
2 - Atom nr./grundstof nr. er
Antallet af protoner i et bestemt grundstofs atomkerne er det same so stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u - det er 1/2000 af protonens masse.
Isotoper
I et bestemt grundstofs kerne kan der være et forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoperne er et bestemt grundstof med forskellige masser.
Der findes fx 3 udgaver af grundstoffet hydrogen.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand, H”O. I almindeligt vand indeholder 99,985 % af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015 % tungt vand, men isotopen deuterium.
6 HE - Nukleantal er antallet af atomer inde i kernen (protoner og neutroner)
2 - Atom nr./grundstof nr. er
Antallet af protoner i et bestemt grundstofs atomkerne er det same so stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u - det er 1/2000 af protonens masse.
Isotoper
I et bestemt grundstofs kerne kan der være et forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoperne er et bestemt grundstof med forskellige masser.
Der findes fx 3 udgaver af grundstoffet hydrogen.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand, H”O. I almindeligt vand indeholder 99,985 % af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015 % tungt vand, men isotopen deuterium.
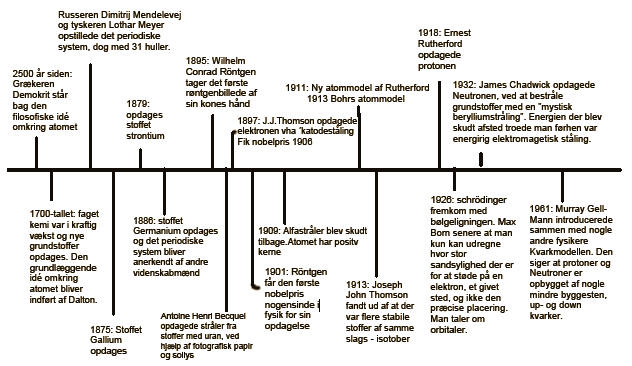
Atomets opbygning
Oprindelig forestillede man sig, at atomet
var en lille kugle, som ikke kunne deles i mindre dele. Ordet atom kommer af
det græske ord atomos, som betyder udelelig.
Fra slutningen af 1800-tallet og
frem til starten af 1900-tallet udførte betydningsfulde fysikere forskellige
forsøg, der betød at forestillingen om atomet flere gange blev taget op til
fornyet overvejelse. Det er udfaldet af alle disse forsøg, der er grundlaget
for vores nutidige viden og forestilling om atomets opbygning.
Atomer og det periodiske system
Protonerne og neutronerne sidder inde i kernen, og elektronerne sidder ude på skallen. Elektrontallet kan varierer, men det kan protontallet ikke - derfor kan man se på antallet af protoner, hvilket grundstof det er.
6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er
atomnummeret/grundstofnummeret
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
Antallet af protoner i et bestemt grundstofs atomkerne er det samme som stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u. Det er 1/2000 af protonens masse.
Isotoper
I et bestemt grundstofs kerne kan der være et forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoperne er et bestemt grundstof med forskellige masser.
Der findes fx 3 udgaver af grundstoffet hydrogen.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand, H”O. I almindeligt vand indeholder 99,985 % af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015 % tungt vand, men isotopen deuterium.
Massen af 1 ml almindeligt vand er præcis 1 gram, men samme mængde tungt vand med to deuterium-isotoper i molekylet har massen 1,11 g.
6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er
atomnummeret/grundstofnummeret
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
Antallet af protoner i et bestemt grundstofs atomkerne er det samme som stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u. Det er 1/2000 af protonens masse.
Isotoper
I et bestemt grundstofs kerne kan der være et forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoperne er et bestemt grundstof med forskellige masser.
Der findes fx 3 udgaver af grundstoffet hydrogen.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand, H”O. I almindeligt vand indeholder 99,985 % af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015 % tungt vand, men isotopen deuterium.
Massen af 1 ml almindeligt vand er præcis 1 gram, men samme mængde tungt vand med to deuterium-isotoper i molekylet har massen 1,11 g.
Kopiside 1.4
Grundstof på engelsk?
Element
Det periodiske system på engelsk?
The periodic table
Det engelske navn for...?
Bly: Lead
Kalium: Potassium
Kviksølv: Mercury/quicksilver
Jern: Iron
Kobber: Copper
Natrium: Sodium
Hvad hedder silicon og sulfur på dansk?
Silicon: Silicium
Sulfur: Svovl
Hvad hedder hydrogen og oxygen på svensk?
Hydrogen: Väte
Oxygen: Syre
Atom navn, protoner, neutroner, nukleoner i 48,22 Ti:
Atomnavnet er Titan.
Der er 22 protoner.
Der er 26 neutroner
Der er 48 nukleoner.
Formlen for almindeligt og tungt hydrogen:
Almindeligt hydrogen: 1,1 H
Tungt hydrogen: 2, 1 H
Neutroner som hver jern-isotop har, når de har 54, 56 og 57 nukleoner:
Jern-isotop med 54 neutroner = 28 neutroner
Jern-isotop med 56 neutroner = 30 neutroner
Jern-isotop med 57 neutroner = 31 neutroner
Hvor mange stabile isotoper findes der af guld, standardformlen:
Der er en stabil isotop.
197, 79 AU.
Hvilket stof har ni stabile isotoper?
Det er grundstoffet Xenon der har ni isotoper. Det er grundstof nr. 54.
Oxygen har 3 stabile isotoper. Hvilken isotop er der mest af?
Den første, er den almindelige, med 8 protoner og 8 neutroner.
Den anden har 8 protoner og 9 neutroner.
Den sidste har 8 protoner og 10 neutroner.
5 grundstoffer der kun har 1 stabil isotop, på de første 3 rækker:
Den første er beryllium, så Fluorine, Sodium/Natrium, Aluminium og Phosphorus/Fosfor
Hvor mange protoner er der i sølv-atomets kerne?
Der er 47 protoner i sølv-atomets kerne.
Hvad er navnet og nummeret på Hg, Nb og P?
Nb = Niobium, nummer 41.
P = Fosfor, nummer 15.
Hg = Kviksølv, nummer 80.
Hvilke grundstof har flest stabile isotoper?
Tin har flest stabile isotoper - nemlig i alt 10 isotoper.
Hvilke grundstof med et nummer under 82 har ikke stabile isotoper?
Grundstof nummer 43, Technetium
Grundstof på engelsk?
Element
Det periodiske system på engelsk?
The periodic table
Det engelske navn for...?
Bly: Lead
Kalium: Potassium
Kviksølv: Mercury/quicksilver
Jern: Iron
Kobber: Copper
Natrium: Sodium
Hvad hedder silicon og sulfur på dansk?
Silicon: Silicium
Sulfur: Svovl
Hvad hedder hydrogen og oxygen på svensk?
Hydrogen: Väte
Oxygen: Syre
Atom navn, protoner, neutroner, nukleoner i 48,22 Ti:
Atomnavnet er Titan.
Der er 22 protoner.
Der er 26 neutroner
Der er 48 nukleoner.
Formlen for almindeligt og tungt hydrogen:
Almindeligt hydrogen: 1,1 H
Tungt hydrogen: 2, 1 H
Neutroner som hver jern-isotop har, når de har 54, 56 og 57 nukleoner:
Jern-isotop med 54 neutroner = 28 neutroner
Jern-isotop med 56 neutroner = 30 neutroner
Jern-isotop med 57 neutroner = 31 neutroner
Hvor mange stabile isotoper findes der af guld, standardformlen:
Der er en stabil isotop.
197, 79 AU.
Hvilket stof har ni stabile isotoper?
Det er grundstoffet Xenon der har ni isotoper. Det er grundstof nr. 54.
Oxygen har 3 stabile isotoper. Hvilken isotop er der mest af?
Den første, er den almindelige, med 8 protoner og 8 neutroner.
Den anden har 8 protoner og 9 neutroner.
Den sidste har 8 protoner og 10 neutroner.
5 grundstoffer der kun har 1 stabil isotop, på de første 3 rækker:
Den første er beryllium, så Fluorine, Sodium/Natrium, Aluminium og Phosphorus/Fosfor
Hvor mange protoner er der i sølv-atomets kerne?
Der er 47 protoner i sølv-atomets kerne.
Hvad er navnet og nummeret på Hg, Nb og P?
Nb = Niobium, nummer 41.
P = Fosfor, nummer 15.
Hg = Kviksølv, nummer 80.
Hvilke grundstof har flest stabile isotoper?
Tin har flest stabile isotoper - nemlig i alt 10 isotoper.
Hvilke grundstof med et nummer under 82 har ikke stabile isotoper?
Grundstof nummer 43, Technetium