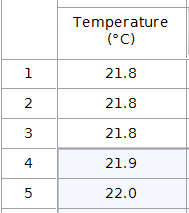
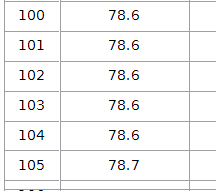
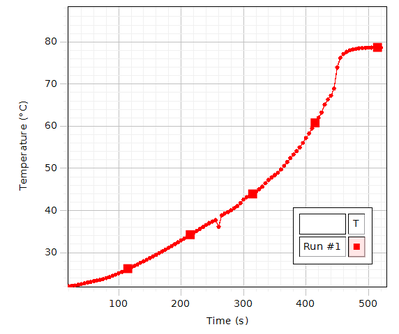
2.1 Ethanols kogepunkt:
Opstilling: Vi tager en bunsenbrænder og et stativ, hvor vi sætter et termometer og et reagensglas fast på. Som vist på billedet nedenunder. Vi tager også et bæger glas, som vi fylder næsten halvt med vand, da reagensglasset skal være i et vandbad. I reagenglasset hælder vi ca. 2 centimeter sprit/ethanol i.
Derefter tænder vi bunsenbrænderen, og skal finde ud af hvor mange grader dampen fra spritten kan være, for at det koger. Det vi kan konkludere er, at ethanol koger ved ca. 78,7 grader, det gør det efter 5 minutter og 26 sekunder. Termometeret skal være ca. 1-2 centimeter fra væsken, da det er dampen vi skal måle temperaturen på, og derfor må termometeret ikke røre ved reagensglassets sider.
Alkohol i hverdagen
Alkohol, ethylalkohol, ethanol, vinånd, sprit, generel betegnelse for den mest kendte af alle alkoholer: ethanol.
Alkohol bliver brugt rigtig meget i hverdagen. Man bruger selvfølgelig alkohol til drikkevarer, som fx vin, øl, mokai, rom osv. Man kan også bare alkohol til medicins, og stærke midler man kan gøre rent med. Når man bruger det til fx stærke midler at gøre rent med, kan det være i form af sprit. Sprittet bliver blandet i produktet, det kan godt bare være ren sprit, men det er for det meste blandet op med andre kemiske midler.
Alkohol er ikke sundt at drikke. Det er skadeligt for din lever og hjerte. Man har større risiko for kræft, hvis man drikker meget alkohol, da det går ud over de organer alkoholen rammen. Så man vil få størst risiko for at få kræft i halsen, munden, leveren, nyren, tyktarmen og endetarmen.
Alkohol kan være et stort problem for unge og voksne. Nogen kan ikke styre det, og det kan være med forsage, at folk bliver alkoholiker. Det er en sygdom, som er svært at komme af med. I de værste tilfælde dør en alkoholiker efter lang tid kroppen har været på overarbejde. Alkoholiker ødelægger deres krop. De ødelægger leveren, og leveren er den der renser kroppen, så til sidst kan kroppen ikke følge med, og der ender med at være alt for mange affaldsstoffer i kroppen, som kroppen ikke kan nedbryde. Så går man i leverkoma, og er man uheldig så dør man.
Alkohol kan også føre til trafikulykker, selvmord, druk, vold osv. Når man har fået alkohol i blodet, har man svært ved at kontrollere kroppen, og det kan så føre til ting der ikke burde være sket, hvis man ikke havde haft alkohol i blodet.
Alkohol / entanol er både smart indenfor medicin, og midler til at gøre rent med. Men alkohol kan også være rigtig grusomt, så der er både fordele og ulemper ved alkohol.
Alkohol, ethylalkohol, ethanol, vinånd, sprit, generel betegnelse for den mest kendte af alle alkoholer: ethanol.
Alkohol bliver brugt rigtig meget i hverdagen. Man bruger selvfølgelig alkohol til drikkevarer, som fx vin, øl, mokai, rom osv. Man kan også bare alkohol til medicins, og stærke midler man kan gøre rent med. Når man bruger det til fx stærke midler at gøre rent med, kan det være i form af sprit. Sprittet bliver blandet i produktet, det kan godt bare være ren sprit, men det er for det meste blandet op med andre kemiske midler.
Alkohol er ikke sundt at drikke. Det er skadeligt for din lever og hjerte. Man har større risiko for kræft, hvis man drikker meget alkohol, da det går ud over de organer alkoholen rammen. Så man vil få størst risiko for at få kræft i halsen, munden, leveren, nyren, tyktarmen og endetarmen.
Alkohol kan være et stort problem for unge og voksne. Nogen kan ikke styre det, og det kan være med forsage, at folk bliver alkoholiker. Det er en sygdom, som er svært at komme af med. I de værste tilfælde dør en alkoholiker efter lang tid kroppen har været på overarbejde. Alkoholiker ødelægger deres krop. De ødelægger leveren, og leveren er den der renser kroppen, så til sidst kan kroppen ikke følge med, og der ender med at være alt for mange affaldsstoffer i kroppen, som kroppen ikke kan nedbryde. Så går man i leverkoma, og er man uheldig så dør man.
Alkohol kan også føre til trafikulykker, selvmord, druk, vold osv. Når man har fået alkohol i blodet, har man svært ved at kontrollere kroppen, og det kan så føre til ting der ikke burde være sket, hvis man ikke havde haft alkohol i blodet.
Alkohol / entanol er både smart indenfor medicin, og midler til at gøre rent med. Men alkohol kan også være rigtig grusomt, så der er både fordele og ulemper ved alkohol.
3.1 Antændelse af alkohol
20% alkohol: Kan ikke antændelse
35% alkohol: Antændes efter opvarmning
40% alkohol: Antændes efter opvarmning
45% alkohol: Antændes efter opvarmning
60% alkohol: Antændes uden opvarmning
80% alkohol: Antændes uden opvarmning
Billedet nedenunder er antændelsen af 80% alkohol
35% alkohol: Antændes efter opvarmning
40% alkohol: Antændes efter opvarmning
45% alkohol: Antændes efter opvarmning
60% alkohol: Antændes uden opvarmning
80% alkohol: Antændes uden opvarmning
Billedet nedenunder er antændelsen af 80% alkohol

Man tager en teske, hvor man skifter mellem de forskellige procenter alkohol, hvor man tager 10-20 dråber af hver. Man kan se at jo højere procenten er, er det lettere for ethanolen at brænde uden opvarmning. Jo lavere procenten er, kan det enten ikke brænde eller så skal det opvarmes først, før alkoholen kan brænde.
6.1 Alkoholgæring

<-- Dette forsøg er opstillet som vist på dette billede. Meningen med dette forsøg er, at man skal skille ethanolen fra gæringen. Ethanolen skilles fra gæringen ved fordampning.

Man starter med at opvarme gæringen op, og det er vigtigt at den hele er mellem de 78-88 grader. Det er også meget vigtigt, at temperaturen er meget jævn, for ellers virker gæringen ikke optimalt, og glasset kan risikere at sprænge. Når temperaturen er høj nok, begynder ethanolet langsomt at sive op i et glas rør, som sidder i proppen, som er sat op en kolbe. Efter det er sivet op i glasrøret, siver ethanolet videre ned gennem slangen og til aller sidst ned i et reagensglas. Som det ses på billedet, er reagensglasset placeret i et glas fuldt med vand i, som også er nedkølet af isterninger. Det gør man, fordi det skal blive til vand og ikke gas. Dette forsætter man så bare med i noget tid, og langsomt kommer der mere og mere ethanol i reagensglasset. Det er en meget langsom proces, som kræver tid.

<-- dette var det vi nåede, at opsamle. Vi nåede cirka 1 cm på cirka 25 min.
Volumenprocent eller vægtprocent
Volumen --> Rumfang
Vægt --> Hvor meget det vejer
Ethanols massefylde ( cirka ) = 0,8 g/ml
Hvad vejer 500 ml ethanol : 400 g
Hvad vejer 500 ml vand : 500 g
Det vil sige, at vand vejer mere end ethanol - Ethanol fylder mindre end vand.
500 ml vand + 500 ml ethanol = 960 ml
Man vil tro, at det vil give 1000 ml, men det giver kun 960 - da ethanol fylder mindre.
For at finde de forskellige procenter
500 ml vand blandet med 500 ml ethanol giver altså :
* en vægt på 900 g
* en volumen på 960 ml
Hvor mange procent udgør 400 ( ren ethanol ) g af 900 ( vand og ethanol ) g?
400 / 900 * 100 = 44,44 %
Hvor mange procent udgør 500 ( ren ethanol ) ml af 960 ( ethanol og vand ) ml ?
500/960* 100 = 52,08
Så kan vi konkludere, at volumen er højest - det er volumen man bruger når man skal skrive på alkohols flasker.
Konklusion af alkohol
Ethanol er
* farveløs væske
*Kogepunkt = 78 grader
*Frysepunkt = -117
*massefylde = 0,795 g/ml
- Ethanol til alkohol C2H50H - når endelsen er 0H er det et alkohol.
- Molekyler, hvor der indgår carbonatomer defineres som organiske forbindelser - Ethanol er en organisk forbindelse
- 2 undtagelser : CO2 ( carbondioxid kuldioxid ) og CO ( kulmonooxid )
- Når ethanol forkemmer en fuldstædig forbrænding
afstemmes
C2H5OH + 0 _____________ CO2 ( indikator for kalkvand ) + H2O ( hvidt / blåt CUSO4 )
Ånding er en fuldstændig forbrænding - der dannes i vand og kuldioxid ( respiration )
Reaktionsskema respiration og fotosyntese
Kalkvand - Ca(OH) --> kan bruges som indikator for CO2
Når Calcirmhydropxid reagerer med kuldioxid vil der dannes et hvid uopløseligt bundfald
Calciumcarbonat - CaCO3
Gæring og destillation
Ethanol dannes ved en kemisk proces, når glukose(druesukker), C6H12O6 under oxygenfrie forhold er i kontakt med bage gær. Samtidig dannes carbondioxid, der er en gas. Når gærbrød hæves, skyldes det netop carbondioxid, dannet ved gæring af sukker. Reaktionsskemaet ser sådan ud:
C6H12O6 à2 C2H5OH + 2 CO2
Druesukker - ethanol - kuldioxid
Gæringsprocessen foregår bedst muligt under en lun temperatur og når gæret får produceret nok ethanol ca. 12-14% vil gæren dræbe sig selv
Ved destillationen udnytter vi det at ethanol og vand har forskellige kogepunkt, og derved kun opvarme så ethanolen fordamper. Derved kan vi producere næsten ren ethanol. Vores destillat nåede en alkoholprocent på ca. 55%
Man vil aldrig kunne producere 100% ren ethanol, der vil altid være lidt vand bundet til alkoholen, derfor er det fineste man kan opnå ca. 96-98% ren ethanol.
5.1 Ethanol til ethanal
Reaktionsskemaet: 2 CH3CH2OH+O2à 2 CH3CHO + 2 H2O
Ethanol Ethanal
Cu = katalysator
Ethanal kan påvirkes med en alon-indikator - Aldelyd
12.1 Ethanol til ethen
Reaktionsskemaet: C2H5OHà C2H4+H2O
Ethanol kan meget nemt omdannes til kulbrinten ethen.
Ethanol dannes ved en kemisk proces, når glukose(druesukker), C6H12O6 under oxygenfrie forhold er i kontakt med bage gær. Samtidig dannes carbondioxid, der er en gas. Når gærbrød hæves, skyldes det netop carbondioxid, dannet ved gæring af sukker. Reaktionsskemaet ser sådan ud:
C6H12O6 à2 C2H5OH + 2 CO2
Druesukker - ethanol - kuldioxid
Gæringsprocessen foregår bedst muligt under en lun temperatur og når gæret får produceret nok ethanol ca. 12-14% vil gæren dræbe sig selv
Ved destillationen udnytter vi det at ethanol og vand har forskellige kogepunkt, og derved kun opvarme så ethanolen fordamper. Derved kan vi producere næsten ren ethanol. Vores destillat nåede en alkoholprocent på ca. 55%
Man vil aldrig kunne producere 100% ren ethanol, der vil altid være lidt vand bundet til alkoholen, derfor er det fineste man kan opnå ca. 96-98% ren ethanol.
5.1 Ethanol til ethanal
Reaktionsskemaet: 2 CH3CH2OH+O2à 2 CH3CHO + 2 H2O
Ethanol Ethanal
Cu = katalysator
Ethanal kan påvirkes med en alon-indikator - Aldelyd
12.1 Ethanol til ethen
Reaktionsskemaet: C2H5OHà C2H4+H2O
Ethanol kan meget nemt omdannes til kulbrinten ethen.